Эйкозаноиды: история открытия и физиологические свойства
Эйкозаноиды – это группа биологически активных соединений, в которую входят простаноиды (простагландины, простоциклины, тромбоксаны) и лейкотриены. В силу своей уникальной структуры и функциональных особенностей эйкозаноиды играют важную роль в регуляции различных физиологических процессов.
Существование эйкозаноидов стало известно еще в начале прошлого века, когда было обнаружено, что экстракты парных половых желез и предстательной железы многих видов животных оказывают гипотензивный эффект. В то же время существование «неизвестного сосудистого гормона», который мог бы объяснить этот эффект, оставалось загадкой до 30-х годов.
В 1930 г. американские гинекологи Курцрок и Либ описали сокращение и расслабление изолированной полоски матки человека под действием человеческой спермы. Независимо друг от друга Гольдблатт и Ульф фон Эйлер сообщили об открытии секретов семенных пузырьков предстательной железы, вызывающих сокращение гладких мышц.
Шведский физиолог Ульф фон Эйлер неожиданно обнаружил в 1934-1936 гг., что активное вещество экстрактов предстательной железы и семенной жидкости находится во фракции жирорастворимых кислот, которые он назвал простагландинами (от prostate gland).
Эйлер описал некоторые фармакологические свойства активного экстракта, предположив, что простагландины играют важную роль в организме. Но поскольку уровень аналитических способов исследования был недостаточен, вещество выделить чистым видом и изучить его химическую структуру не удалось.
В настоящее время структура и механизмы действия эйкозаноидов достаточно хорошо изучены. Простагландины, простоциклины и тромбоксаны участвуют в регуляции тромбообразования, контроле артериального давления и гладких мышц. Лейкотриены связаны с различными типами воспалительной реакции и аллергии.
Исследование простагландинов
Изначальный интерес к простагландинам был связан с их ролью в процессе родов, так как тогда было замечено, что простагландин увеличивает силу и частоту сокращения матки у беременных женщин. Работы в этой области велись еще в начале ХХ века, но настоящий прорыв произошел только в 1942 г., когда Бергсли и Мазерс сообщили о выделении активного вещества — определившегося позднее как простагландин — из культур микроорганизмов Aspergillus niger.
Работу над простагландинами продолжил ученик Эйлера С. Бергстрем, перед которым стояла задача выделить в кристаллическом виде активное начало, т.е. простагландин, из экстрактов простаты и семенной жидкости баранов. Вначале С. Бергстрему удалось сделать немногое: он выяснил только, что простагландин находится во фракциях вместе с ненасыщенными жирными оксикислотами, и вынужден был прервать дальнейшие исследования на несколько лет.
Жизнь и творчество эйлера
... Это научно-популярная энциклопедия широкого охвата, написанная ярко и общедоступно.[L 7] По отзывам современников, Эйлер всю жизнь оставался скромным, жизнерадостным, чрезвычайно отзывчивым человеком, всегда ... вариационного исчисления». Именно здесь впервые появилось название нового раздела математики, созданного Эйлером и Лагранжем. В 1762 году на русский престол вступила Екатерина II, которая ...
Одной из главных причин, обусловивших этот перерыв, были затруднения с исходным материалом для выделения простагландинов — везикулярными железами барана, самым богатым простагландинами источником. Но поскольку уже к тому времени биохимики и фармакологи заинтересовались простагландинами, в 1956 г. в ряде стран северного полушария была организована специальная программа исследований простагландинов, в которую вошел и сбор замороженных везикулярных желез барана.
Уже в следующем году С. Бергстрем и Дж. Шьевалл получили несколько миллиграммов индивидуального вещества в кристаллическом состоянии и назвали его простагландин F за его растворимость в фосфатном буфере. Полученного количества хватило лишь на то, чтобы установить, что простагландин F — это ненасыщенная жирная кислота, определить температуру его плавления и продемонстрировать способность в концентрации всего 5*10-9 г в 1 мл раствора давать хороший эффект по сокращению гладкой мышцы.
Затем в кристаллическом же состоянии было получено еще одно вещество подобного типа — простагландин Е (обозначение возникло от слова ester — эфир, которым извлекался этот простагландин).
Оба соединения были одинакового молекулярного веса и очень сходного строения, но в корне различались биологическими свойствами: простагландин Е понижал кровяное давление, а простагландин F сокращал гладкую мускулатуру.
Работы по простагландинам развивались быстрыми темпами, и за 1972 — 1976 годы С. Бергстрем, Б. Самуэльссон и Дж. Вейн получили в чистом виде еще 10 простагландинов, установили их структуру и определили биологические свойства. В 1979 г. Б. Самуэльссон с коллегами открыл еще один тип соединений — близкие простагландинам лейкотриены.
Выделение простагландинов, изучение структуры и свойств — работа чрезвычайно трудная: мало того что их концентрации в объектах выделения очень низки, вещества эти крайне неустойчивы, они теряют свою биологическую активность, по которой следят за веществом в ходе его выделения, в течение 1 — 2 мин. Недаром за исследования простагландинов С. Бергстрему, Б. Самуэльссону и Дж. Вейну в 1982 г. была присуждена Нобелевская премия.
A, B, C, D, E, F, G, I.
Субстраты для синтеза эйкозаноидов
Главный субстрат для синтеза эйкозаноидов у человека — арахидоновая кислота, так как её содержание в организме человека значительно больше остальных полиеновых кислот — предшественников эйкозаноидов.
В образовании эйкозанондов принимают участие также и другие незаменимые жирные кислоты (линолевая и а-линоленовая), но только после элонгации на два углеродных атома и десатурацнн, т.е. после превращения в 20-углеродные тетраеновые кислоты. Арахидоновая, 8,11,14-эйкозатриеновая и 5,8,11,14,17-эйкозапентаеновая кислоты — предшественники эйкозаноидов.
Полиеновые кислоты с 18 и 20 атомами углерода поступают в организм человека с пищей или образуются из незаменимых (эссенциальных) жирных кислот с 18 атомами углерода. (Рис.1)
Интересные факты о серии книг «Жизнь замечательных людей»
... таких мелочей и строится жизнь. Другие темы: ← Общение↑ На свободную темуВолонтерство → ` Эссе ЕГЭ Д.С. Лихачёв. «Письма о добром и прекрасном»., Письмо второе., МОЛОДОСТЬ- ВСЯ ЖИЗНЬ., Темы: дружба, молодость, трудолюбие, ... так отзывался о серии книг ЖЗЛ: « Ни одно из павленковских дел, по моим наблюдениям, не может сравниться с тем огромным влиянием, которое оказала на русских читателей всех ...
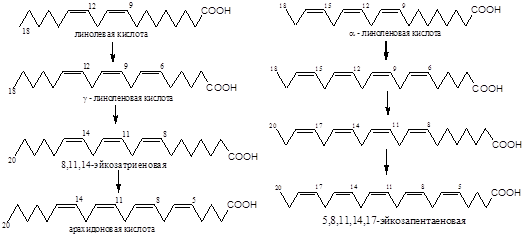
Рис.1. Синтез полиеновых жирных кислот с 20 углеродными атомами в организме человека.
Полиеновые жирные кислоты, которые могут служить субстратами для синтеза эйкозаноидов, входят в состав глицерофосфолипидов мембран. Под действием ассоциированной с мембраной фосфолипазы А2 жирная кислота отщепляется от глицерофосфолипида и используется для синтеза эйкозаноидов.
Структура, номенклатура и биосинтез эйкозаноидов
Хотя субстраты для синтеза эйкозаноидов имеют довольно простую структуру (полистовые жирные кислоты), из них образуется большая и разнообразная группа веществ. Наиболее распространены в организме человека простагландины, которые впервые были выделены из предстательной железы, откуда и получили свое название. Позже было показано, что и другие ткани организма синтезируют простагландины и другие эйкозаноиды.
простаноевой
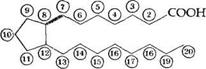
Простагландины обозначают символами, например PG А, где PG обозначает слово «простагландин», а буква А обозначает заместитель в пятичленном кольце в молекуле эйкозаноида.
Обнаружено шесть первичных природных простагландинов, три из них серии Е (PGE 1 , PGE2 , PGE3 ) и три — серии F (PGF1a , PGF2a , PGF3a ).
Простагландины серии Е содержат в положении 9 кетогруппу, а простагландины серии F — гидроксигруппу. (Рис.2)
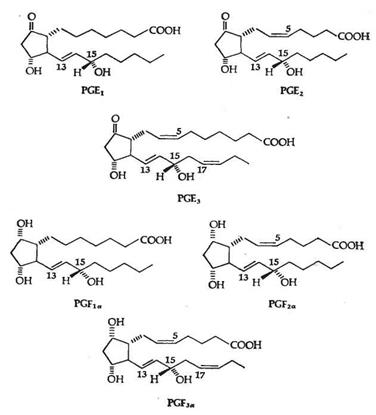
Рис.2 Шесть главных природных простагландинов
В дополнение к вышеприведенным шести первичным простагландинам имеются несколько вторичных простагландинов, большинство из которых являются продуктами ферментативного или химического превращения PGE. Характерным свойством простагландинов серии Е является их способность к дегидратации в PGA в кислой среде; образовавшиеся PGA затем в присутствии оснований изомеризуются в PGB, имеющие максимум поглощения при длине волны 237 нм. Эта последовательность реакций превращения PGE в PGB часто используется для идентификации PGE.
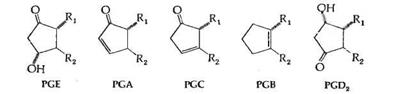
Простагландины серии F не претерпевают подобного превращения в кислой среде.
В зависимости от исходной жирной кислоты все эйкозаноиды делят на три группы:
1) Первая группа образуется из эйкозотриеновой кислоты. Хотя в пищевых продуктах этой кислоты нет, она способна образовываться в клетках при удлинении линолевой кислоты (С18: 3), которой много в растительных маслах. Для этой группы в соответствии с числом двойных связей простагландинам и тромбоксанам присваивается индекс 1: например, PgE 1 , PgI1
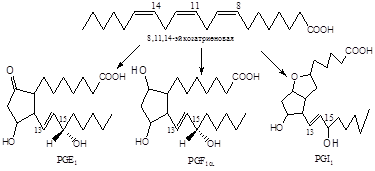
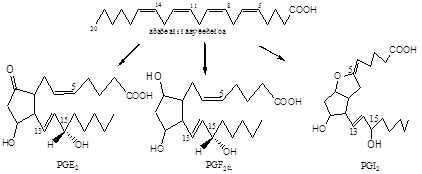
Вторая группа синтезируется из арахидоновой кислоты (С20: 4), по тому же правилу эйкозаноидам этой группы присваивается индекс 2. PgE 2 , PgI2 .
Постмодернизм. Новые виды массового искусства и формы синтеза
... «Йельская школа») и политическими течениями. 1. Постмодернизм в искусстве Исследователи отмечают двойственность постмодернистского искусства: утрату наследия европейских художественных традиций и чрезмерную ... типологический признак. Причем, если в соцреалистическом синтезе различных стилей сохраняется их идентичность, чистота признаков, раздельность, то в постмодернизме можно видеть сплав, ...
Третья группа эйкозаноидов происходит из тимнодоновой кислоты (С20: 5).
Эйкозаноидам этой группы присваивается индекс 3. Например, PgE 3 , PgI3
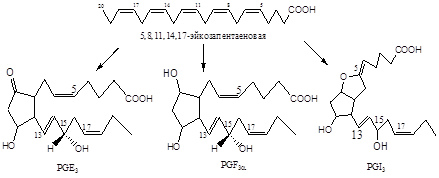
PG I — простациклины. Имеют 2 кольца в своей структуре: одно пятичленное, как и другие простагландины, а другое — с участием атома кислорода. Их также подразделяют в зависимости от количества двойных связей в радикалах (PG I 2 , PG I3 ).
Тромбоксаны. В отличие от простагландинов, тромбоксаны синтезируются только в тромбоцитах, откуда и происходит их название, и стимулируют их агрегацию при образовании тромба.
Тромбоксаны имеют шестичленное кольцо, включающее атом кислорода. Так же, как и другие эйкозаноиды, тромбоксаны могут содержать различное число двойных связей в боковых цепях и отличающиеся по активности. ТХ В 2 — продукт катаболизма ТХ А2 и активностью не обладает.
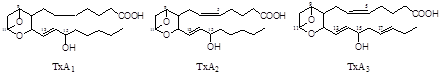
Рис.3. Структура тромбоксанов.
Биосинтез
После отделения арахидоновой кислоты от фосфолипида она выходит в цитозоль и в различных типах клеток превращается в разные эйкозаноиды. В клетках имеется 2 основных пути превращения арахидоновой кислоты: циклооксигеназный, приводящий к синтезу простагландинов, простациклинов и тромбоксанов, и липоксигеназный, заканчивающийся образованием лейкотриенов. (Рис.4)
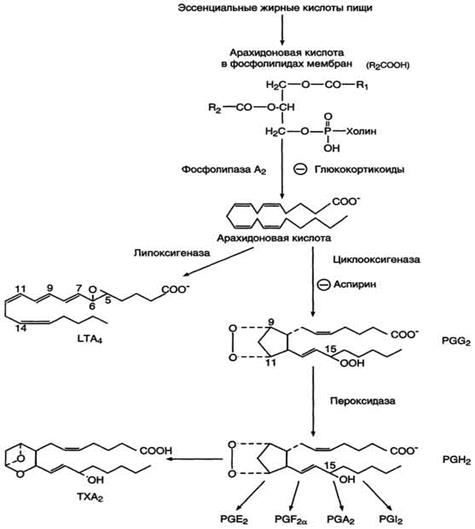
Рис.4 Синтез эйкозаноидов из арахидоновои кислоты.
Циклооксигеназный путь: синтез простагландинов и тромбоксанов
простагландинсинтазы.
Фермент, катализирующий первый этап синтеза простагландинов, называется PG Н2 синтазой и имеет 2 каталитических центра. Один из них называют циклооксигеназой, другой — пероксидазой. Этот фермент представляет собой димер гликопротеинов, состоящий из идентичных полипептидных цепей. Фермент имеет гидрофобный домен, погружённый в липидный слой мембран ЭР, и каталитический домен, обращённый в полость ЭР. В активном центре циклооксигеназы находится тирозин (385), в активном центре пероксидазы — простетическая группа — гем. В организме имеются 2 типа циклооксигеназ (PGН 2 синтаз).
Циклооксигеназа 1 — конститутивный фермент, синтезирующийся с постоянной скоростью. Синтез циклооксигеназы 2 увеличивается при воспалении и индуцируется соответствующими медиаторами — цитокинами. Оба типа циклооксигеназ катализируют включение 4 атомов кислорода в арахидоновую кислоту и формирование пятичленного кольца. В результате образуется нестабильное гидропероксидпроизводное, называемое PG G2 . Гидропероксид у 15-го атома углерода быстро восстанавливается до гидроксильной группы пероксидазой с образованием PG Н2 . До образования PG Н2 путь синтеза разных типов простагландинов одинаков. Дальнейшие превращения PG Н2 специфичны для каждого типа клеток.
«Синтез искусств в эстетическом воспитании школьников» материал по музыке
... прекрасного, повышать духовность. Все выше изложенное и определило актуальность темы данной курсовой работы: «Синтез искусств на уроках музыки». Цель - изучение проблем гармоничного развития ... подчиняющий единому замыслу элементы изобразительного искусства, словесного творчества, музыки, а также обрядовые действия, выступает как организующее начало синтеза искусств, начиная с культур Древнего ...
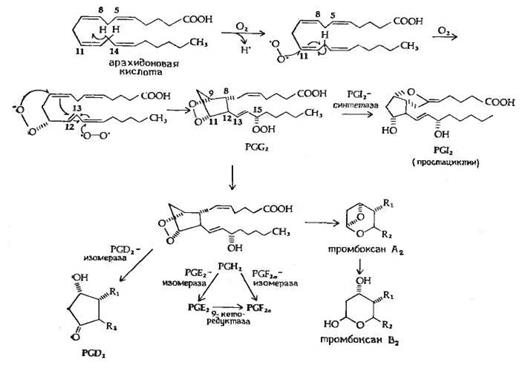
Рис.5. Предполагаемый механизм биосинтеза PGE 2 и PGF2 a из арахидоновой кислоты.
Биосинтез PGE 2 и PGF2 a , представленный на рис.5, начинается с арахидоновой кислоты и катализируется циклооксигеназой ( М 70 000) жирных кислот, при этом образуется 15-оксиперокси-9-11-эндопероксид PGG2 . Первая стадия в этой последовательности реакций приводит к потере атома водорода у С-13 с образованием свободного радикала. Эта стадия лимитирует скорость всего процесса. Затем происходят присоединение пероксидного радикала в положения 9 и 11 и образование 8,12 углерод-углеродной связи, которому предшествует изомеризация 11,12-двойной связи в 12,13-двойную связь и присоединение другого пероксидного радикала в положение 15, приводящее к изомеризации 12,13-двойной связи в 13,14-двойную связь. Все эти превращения рассматриваются как процесс одноэлектронного переноса, обозначенный на рисунке изогнутыми стрелками. Первый продукт этой последовательности реакций — это 15-оксиперокси-9,11-эндопероксид PGG2 , существование которого было постулировано за несколько лет до его выделения и идентификации. PGG2 затем превращается в PGI2 или PGH2 , вероятно, с помощью реакции пероксидазного типа. PGH2 является предшественником PGE2 и PGF2 a в семенных пузырьках и других органах, а также тромбоксана А2 в тромбоцитах и легких.
Превращение арахидоновой кислоты в PGG 2 блокируется ингибиторами циклооксигеназы жирных кислот. Наиболее известным среди этих ингибиторов являются аспирин (ацетилсалициловая кислота) и ряд других противовоспалительных лекарств (Рис.6).
Торможение аспирином обусловлено переносом ацетильного остатка от молекулы аспирина к активному центру фермента с инактивацией последнего; такого рода механизм был предложен в качестве объяснения некоторых известных фармакологических эффектов аспирина.
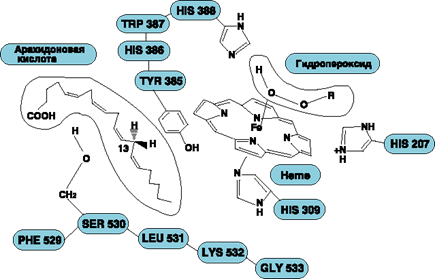
Рис.6. Молекулярный механизм ингибирования циклооксигеназы ацетилсалициловой кислотой.
Введение
Воспаление является одним из основных процессов, возникающих в организме в ответ на различные воздействия. Оно сопровождается рядом характерных признаков, таких как опухоль, покраснение, повышение температуры и боль. Для снижения воспалительной реакции и облегчения симптомов применяются различные противовоспалительные препараты.
Аспирин и его механизм действия
Аспирин является одним из наиболее широко используемых противовоспалительных препаратов. Его эффективность объясняется его способностью подавлять основные признаки воспаления. Механизм противовоспалительного действия аспирина был объяснен открытием его способности ингибировать циклооксигеназу — фермент, играющий ключевую роль в синтезе медиаторов воспаления.
Циклооксигеназа ингибируется аспирином путем ацетилирования серина в положении 530 в активном центре фермента. Это приводит к уменьшению синтеза медиаторов воспаления и, следовательно, снижению воспалительной реакции.
«Огонь, мерцающий в сосуде…» (Красота в жизни и искусстве)
... А может быть, и то и другое вместе? Что важнее и в жизни, и в искусстве -- форма или содержание? С.И.Ожегов раскрывает содержание слова «красота» так: «Все красивое, прекрасное, всё то, что ... В своём реферате я рассматриваю вопросы, связанные с проявлением красоты в природе, в человеке, в отношениях и поступках человека и в искусстве. I. «О красоте в жизни» 1.1 Красота в природе «Природа нравится и ...
Однако эффект действия аспирина ограничен во времени, так как экспрессия гена циклооксигеназы не нарушается, и продуцируются новые молекулы фермента. Поэтому аспирин не обеспечивает длительное противовоспалительное действие.
Другие нестероидные противовоспалительные препараты
Кроме аспирина, существует ряд других нестероидных противовоспалительных препаратов, таких как ибупрофен и ацетаминофен. Они действуют по конкурентному механизму, связываясь с активным центром циклооксигеназы и уменьшая синтез медиаторов воспаления.
Таким образом, эти препараты также способны снижать воспалительную реакцию и облегчать симптомы воспаления.
Стероидные противовоспалительные препараты
В отличие от нестероидных противовоспалительных препаратов, стероидные препараты обладают гораздо более сильным противовоспалительным действием. Их механизм действия заключается в индукции синтеза белков — липокортинов, которые ингибируют активность фосфолипазы А2 и уменьшают синтез всех типов эйкозаноидов.
Эйкозаноиды — это группа биологически активных веществ, включающая простагландины и лейкотриены, которые играют ключевую роль в развитии воспаления.
Структура и синтез лейкотриенов являются важными мишенями для стероидных противовоспалительных препаратов. Они препятствуют освобождению субстрата для синтеза эйкозаноидов — арахидоновой кислоты, что приводит к снижению синтеза лейкотриенов.
Применение стероидных противовоспалительных препаратов
Использование стероидных противовоспалительных препаратов особенно важно для больных, страдающих бронхиальной астмой. Это заболевание характеризуется развитием симптомов, таких как бронхоспазм и экссудация слизи в просвет бронхов.
Одной из причин развития «аспириновой» бронхиальной астмы является избыточная продукция лейкотриенов клетками, такими как тучные клетки, лейкоциты и клетки эпителия бронхов. Прием аспирина у больных с высокой активностью липоксигеназы может вызвать приступ бронхиальной астмы.
В отличие от аспирина и других нестероидных противовоспалительных препаратов, стероидные препараты ингибируют использование арахидоновой кислоты и по липоксигеназному и по циклооксигеназному пути. Поэтому они не способны вызывать бронхоспазма.
Заключение
Противовоспалительные препараты, такие как аспирин, нестероидные препараты и стероиды, имеют различные механизмы действия, но объединяются общей целью — снижением воспалительной реакции в организме. Каждый из этих препаратов имеет свои особенности и применяется в зависимости от типа и тяжести воспалительного процесса.
Наличие 3 сопряжённых двойных связей обусловливает название «лейкотриен». Лейкотриены также образуются из эйкозаноевых кислот, однако в их структуре отсутствуют циклы, как у простагландинов, и они имеют 3 сопряжённые двойные связи, хотя общее число двойных связей в молекуле больше (рис.7).
Лейкотриены С 4 , D4 и Е4 имеют заместители в виде трипептида глутатиона, дипептида глицилцистеина или цистеина, соответственно.
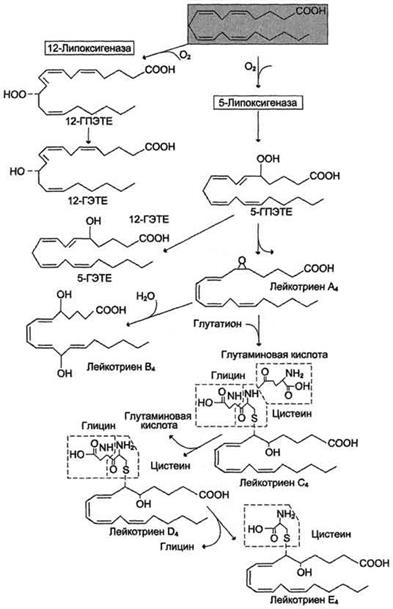
Рис.7. Липоксигеназный путь синтеза эикозаноидов.
Синтез лейкотриенов идёт по пути, отличному от пути синтеза простагландинов, и начинается с образования гидроксипероксидов — гидропероксидэйкозатетраеноатов (ГПЭТЕ).
Эти вещества или восстанавливаются с образованием гидроксиэйкозатетроеноатов (ГЭТЕ) или превращаются в лейкотриены. ГЭТЕ отличаются по положению гидроксильной группы у 5-го, 12-го или 15-го атома углерода, например: 5-ГЭТЕ, 12-ГЭТЕ.
Липоксигеназы действуют в 5-й, 12-й или 15-й позиции арахидоновой кислоты в зависимости от типа ткани. Например, в тромбоцитах — 12-липоксигеназа, в эозинофилах — 15-липоксигеназа.
Глюкокортикоиды ингибируют синтез всех типов эйкозаноидов, так как ингибируют фосфолипазу А2, и таким образом уменьшают количество субстрата для их синтеза. Аспирин и другие противовоспалительные препараты нестероидного действия ингибируют только циклооксигеназный путь.
Другие типы лейкотриенов образуются из LTА 4 , LTВ4 образуется под действием эпоксидгидролазы в лейкоцитах и клетках эпителия сосудов. Другой путь приводит к образованию группы лейкотриенов: LTC4 , LTD4 , LTE4 . Их синтез начинается с присоединения трипептида глутатиона к 6-му атому углерода с образованием LTС4 в реакции, катализируемой глутатион-8-трансферазой. В следующей реакции удаляется глутамат, и LTD4 содержит дипептид глицилцистеин. На последней стадии отщепляется глицин, и LTЕ4 содержит только цистеин.
Механизмы действия эйкозаноидов, основные биологические эффекты
Эйкозаноиды — гормоны местного действия по ряду признаков:
Влияние простагландинов на организм
Простагландины — это биологически активные вещества, которые образуются в различных тканях и органах, а не только в эндокринных железах. Они действуют по аутокринному или паракринному механизмам, то есть воздействуют на клетки в той же ткани или в соседних тканях.
Одной из особенностей простагландинов является то, что их концентрация в крови меньше, чем необходимо, чтобы вызвать ответ в клетках-мишенях. Это говорит о том, что в тканях-мишенях присутствует не один-единственный рецептор для простагландинов, а несколько. Более того, различия в характере действия разных видов простагландинов свидетельствуют о том, что небольшие структурные изменения могут иметь большое значение и обусловливать силу и характер ответной реакции.
Простагландины оказывают разнообразное влияние на организм. Они способны вызывать сокращение матки и желудочно-кишечной мускулатуры, регулировать секрецию, транспорт ионов и участвовать в различных метаболических процессах. Интересно, что действие простагландинов на уровень циклического AMP (аденилатциклазы) и уровень Са2+ (кальция) в тканях зависит от вида изучаемой ткани. Это позволяет предполагать, что механизм действия простагландинов включает в себя сложные молекулярные процессы.
Особенно важным является влияние простагландинов на мобилизацию кальция из костей. Простагландины PGE1 и PGE2 значительно ускоряют этот процесс. Интересно, что этот эффект вызывается прямым действием простагландинов и не зависит от гормона паращитовидных желез. Он основан на стимуляции функций остеокластов, клеток, которые рассасывают кость. Избыточное образование простагландинов в злокачественной ткани может объяснять гиперкальцемию и остеолиз, которые наблюдаются у больных некоторыми видами рака.
Механизмы действия эйкозаноидов являются основой для понимания их роли в различных физиологических и патологических процессах. Одним из ключевых механизмов действия эйкозаноидов является их взаимодействие со специальными рецепторами на клетках. Некоторые эйкозаноидные рецепторы связаны с аденилатциклазной системой и протеинкиназой А, что позволяет им воздействовать на клетки через изменение уровня кальция в цитозоле. Так, рецепторы PGE, PGD, PCI, PGF2α, ТХА2 эндоперекисей и лейкотриены влияют на активацию аденилатциклазной системы и уровень кальция в клетках-мишенях.
Наиболее известной функцией эйкозаноидов является их участие в тромбообразовании. В норме эндотелиальные клетки сосудов синтезируют простациклин I2, который препятствует агрегации тромбоцитов и сужению сосудов. Однако, при повреждении стенки сосуда, например, при образовании атеросклеротической бляшки, происходит разрушение клеток эндотелия и снижение синтеза PGI2. Это приводит к активации фосфолипазы А2 и повышению секреции ТХА2, которая стимулирует агрегацию тромбоцитов и образование тромба в области повреждения сосуда.
Избыточная продукция эйкозаноидов может наблюдаться при различных заболеваниях. Понимание механизмов их действия является важным для разработки новых методов лечения и профилактики этих патологических состояний.
В целом, эйкозаноиды оказывают влияние на клетки почти всех тканей организма и выполняют разнообразные функции, включая регуляцию воспалительных процессов, иммунной системы, агрегации тромбоцитов и сокращения сосудов. Дальнейшие исследования в этой области могут привести к расширению наших знаний о биологической роли эйкозаноидов и созданию новых подходов к лечению и профилактике различных заболеваний.
В норме клетки эндотелия продуцируют PG I 2 , который вызывает релаксацию ГМК и ингибирует агрегацию тромбоцитов. Тромбоциты в неактивном состоянии не продуцируют тромбоксаны. В области повреждения стенки сосуда преобладает действие TXА2 , стимулирующего агрегацию тромбоцитов и сокращение стенок сосуда. В результате на повреждённом участке образуется тромб, происходит резкое сужение просвета сосуда. В миокарде это может привести к развитию инфаркта миокарда.
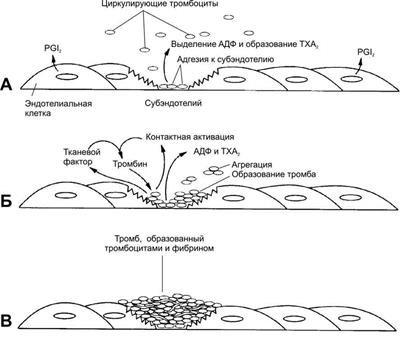
PGI 2 является мощным ингибитором агрегации тромбоцитов, и было показано, что он синтезируется микросомальной фракцией гомогенатов кровеносных сосудов.
PGI 2 обладает двумя важными фармакологическими свойствами, которые обусловливают противодействие PGI2 тромбоксану А2 ; дело в том, что PGI2 является наиболее мощным из всех известных в настоящее время ингибиторов агрегации тромбоцитов и, кроме того, расширяет сосуды. Предполагается, что в результате соприкосновения тромбоцитов с эндотелием нормальных кровеносных сосудов происходит высвобождение PGG2 , субстрата для образования PGI2 ; действие этого механизма способствует предотвращению агрегации тромбоцитов и сужению кровеносных сосудов. Если же тромбоциты вступают в соприкосновение с эндотелием кровеносных сосудов, который имеет разрывы или повреждения вследствие патологических изменений, то из-за недостаточной концентрации фермента, катализирующего образование простацнклина PGI2 , количество последнего снижается; при этом агрегирующее действие тромбоксана А2 , который синтезируется из эндопероксида, должно превалировать над антиагрегирующим действием PGI2 , что приводит к тромбозу и местному спазму сосудов.
Действие на сердечно-сосудистую систему
Внутривенное введение PGE 1 или PGE2 увеличивает кровоток путем общего расширения сосудов с уменьшением периферического сопротивления. Эти изменения находят отражение в увеличении сердечного выброса, сопровождающегося уменьшением артериального кровяного давления.
Исследования показали, что потребление большого количества рыбьего жира снижает риск развития инфаркта миокарда. Это связано с тем, что рыбий жир содержит эйкозапентаеновую кислоту (20:5, ω-3), которая играет важную роль в образовании эйкозаноидов, способствующих предотвращению образования тромбов в сосудах сердца.
Когда эйкозапентаеновая кислота поступает в организм с пищей, она включается главным образом в фосфолипиды мембран, а не арахидоновая кислота. После действия фосфолипазы А2 эйкозапентаеновая кислота становится основным субстратом для синтеза эйкозаноидов, которые оказывают существенное влияние на свертываемость крови.
При обычной диете с преобладанием арахидоновой кислоты (20:4, ω-6) действие ТХА2 уравновешивается действием PG I2 и других простагландинов. Однако при диете с преобладанием ω-3 кислот в клетках эндотелия образуются более сильные ингибиторы тромбообразования (PGI3, PGE3, PGD3), что способствует снижению риска образования тромба и развития инфаркта миокарда.
Действие на водно-электролитный обмен
Исследования показали, что все изученные простагландины усиливают ионный поток через эпителиальные мембраны. Например, введение PGE1 или PGA1 в почечную артерию собак приводит к увеличению объема мочи и выделению Na+, K+ и Сl-. С другой стороны, сообщается, что местное образование PGE2 в почке подавляет выведение Na+.
Действие на нервную систему
Простагландины присутствуют в нервной ткани и активируются при раздражении периферических нервов. Исследования показали, что введение простагландинов приводит к повышению температуры тела, а также оказывает седативное и транквилизирующее действие. Кроме того, простагландины являются антагонистами противосудорожных препаратов и модулируют действие норадреналина и других адренергических факторов.
Содержание раздела: Влияние простагландинов на организм человека
Действие на желудочно-кишечный тракт
Простагландины являются универсальными биологически активными веществами, которые оказывают разнообразное воздействие на желудочно-кишечный тракт (ЖКТ).
Кроме того, они играют важную роль в защите слизистой оболочки ЖКТ от патогенных микроорганизмов, регуляции секреции желудка и моторной функции кишечника.
- Простагландины тормозят желудочную секрецию, но стимулируют секрецию поджелудочной железы и секрецию слизи в кишечнике.
- Стимулируя кишечную аденилатциклазу, простагландины могут ингибировать поступление Na+ в клетки слизистой оболочки, что сопровождается увеличением секреции Сl-.
- Эти эффекты в сочетании с увеличением секреции Н2О и кишечной моторики являются основанием для развития вызываемой простагландинами диареи.
Влияние на репродуктивную систему
Простагландины оказывают важное воздействие на репродуктивную систему и используются для различных гинекологических процедур. Например, PGF2a способствует изгнанию плода и плаценты при аборте. К тому же, простагландины являются участниками рождения, регуляции менструального цикла, фертильности и рождаемости.
- Простагландины, особенно PGF2a, стимулируют активность матки в период беременности, что находит применение при вызывании аборта.
- Как invitro, так и invivo PGF2a вызывают рассасывание функционирующего желтого тела и могут облегчить прерывание беременности, уменьшая уровень прогестерона в плазме крови.
Воздействие на бронхи, трахею и гладкие мышцы
Простагландины играют важную роль в регуляции бронхиальной астмы и респираторной функции в целом, обладая способностью вызывать как сокращение, так и расслабление гладких мышц в бронхах и трахее.
- Простагландины серии F вызывают сокращение, а простагландины серии E — раслабление мускулатуры дыхательных путей у людей и животных.
- PGE1 и PGE2 являются мощными бронходилятаторами, т.е. средствами, расширяющими просвет бронхов и бронхиол, при применении их в аэрозолях как у людей, так и у животных, страдающих бронхоспазмами.
- PGF2a вызывает интенсивное сокращение бронхов и бронхоспазм.
Новые данные об эффектах простагландинов и лейкотриенов в развитии воспаления
Простагландины, участвующие в формировании всех компонентов воспаления, выраженно влияют на тонус стенок микрососудов и адгезивно-агрегационные свойства клеток крови.
Недавние исследования выявили, что PGF2 a оказывает воздействие и на гладкие мышцы матки. TG-модулятор, выделяющийся при воспалении и названный rabbitaortacontractingsubstance (RCS), содержит в себе смесь PGG2, PGH2 и тромбоксана А2, при этом важную роль играет тромбоксан А2. Механизм освобождения арахидоновой кислоты из легочной ткани, стимулирующий процесс образования эндопероксидов PG и тромбоксана А2, контролируется декапептидом. Стероидные противовоспалительные средства блокируют освобождающее воздействие RCS и обеспечивают предотвращение процесса образования эндопероксидов и тромбоксана А2, не являясь ингибиторами активности циклооксигеназы.
Лейкотриены оказывают спазмогенное действие на стенки сосудов, бронхиол и кишечник. Однако их положительный хемотаксический эффект по отношению к фагоцитам и повышение мембранной проницаемости являются важными компонентами в процессе развития воспаления. Спазм микрососудов, в особенности артериол, приводит к развитию ишемии, что ухудшает течение воспалительного процесса.
Таким образом, простагландины и лейкотриены имеют множество эффектов в развитии воспаления, в том числе оказывают влияние на кровообращение, агрегацию клеток крови, проницаемость мембран и развитие ишемии. Эти механизмы могут быть использованы для разработки эффективных препаратов против воспалительных заболеваний.
Введение простагландинов подопытным животным увеличивает воспалительную реакцию, вызванную, например, гистамином. Простагландины, образуемые в местах, связанных с повреждением, ожогами или вредными воздействиями, ведут себя как медиаторы воспалительной реакции. Способность таких агентов, как аспирин или другие лекарства, тормозить воспалительную реакцию, связана с их ингибирующим действием на простагландинсинтазу.
Иммунное действие
Ингибирующее действие простагландинов на иммунный ответ объясняется тем, что активация антигенами Т-лимфоцитов, имеющая значение в иммунологическом ответе, ингибируется PGE 1 . В противоположность этому сообщалось, что PGE1 усиливает иммуногенность (способность антигена вызывать иммунный ответ) клеток селезенки как invivo, так и invitro. Кроме того, макрофаги, которые в иммунологических реациях функционируют в тесном взаимодействии с лимфоцитами, изменяя их активность, также продуцируют и секретируют простагландины типа Е. Изучению роли простагландинов в модуляции иммунных реакций придается все большее значение. Предполагают, что продукция простагландинов злокачественными клетками может иметь отрицательные последствия для иммунной системы организма хозяина и, таким образом, может затруднить иммуннотерапевтические подходы к лечению новообразований у человека.
Воздействия на кожу
Воспалительные влияния простагландинов, описанные выше, частично являются результатом их способности вызывать местное увеличение секреции гистамина. В коже подопытных животных наблюдается увеличение проницаемости капилляров, а у человека отмечена стойкая эритема сосудов кожи (сильное покраснение кожи, вызванное расширением капилляров), сопровождаемая появлением волдырей и отека. Это воспалительное действие простагландинов можно предотвратить антивоспалительными агентами, в том числе аспирином.
Таблица 8-8. Характеристика биологического действия основных типов эйкозаноидов
| Эйкозаноид | Основное место синтеза | Основное биологическое действие |
|
PG E 2 |
Большинство тканей, особенно почки | Расслабляет гладкую мускулатуру, расширяет сосуды, инициирует родовую активность, подавляет миграцию лимфоцитов, пролиферацию Т-клеток. |
|
PG F 2 α |
Большинство тканей | Сокращает гладкую мускулатуру, суживает сосуды, бронхи, стимулирует сокращения матки. |
| PG D 3 | Клетки гладкой мускулатуры | Вызывает расширение сосудов, снижает агрегацию тромбоцитов и лейкоцитов. |
|
PG I 2 |
Сердце, клетки эндотелия сосудов | Уменьшает агрегацию тромбоцитов, расширяет сосуды. В клетках-мишенях увеличивает образование цАМФ |
|
TX A 2 |
Тромбоциты | Стимулирует агрегацию тромбоцитов, суживает сосуды и бронхи, в клетках уменьшает образование цАМФ. |
| TX A 3 | Тромбоциты | Обладает функциями, одинаковыми с ТХ А 2 , но значительно менее эффективен. |
| LT B 4 | Лейкоциты, клетки эпителия | Стимулирует хемотаксис и агрегацию лейкоцитов, освобождение лизосомальных ферментов лейкоцитов. Увеличивает проницаемость сосудов. |
| Группа лейкотриенов | Лейкоциты, альвеолярные макрофаги | Стимулируют расширение сосудов, увеличивают их проницаемость. |
Использование производных эйкозаноидов в качестве лекарств
Исследования показывают, что эйкозаноиды являются важными медиаторами в различных биологических процессах, таких как воспалительные реакции, агрегация тромбоцитов, родовая деятельность и другие. Однако, из-за их быстрой инактивации, эйкозаноиды имеют короткий период действия.
Исследования также показывают, что аналоги PGЕ1 и PGЕ2 могут блокировать гистаминовые рецепторы II типа в клетках слизистой оболочки желудка, чем подавляют секрецию соляной кислоты. Н2-блокаторы, включая аналоги эйкозаноидов, ускоряют заживление язв желудка и двенадцатиперстной кишки.
Одним из действий эйкозаноидов является их способность к стимуляции сокращения мускулатуры матки, что может использоваться для стимуляции родовой деятельности.
В ходе исследований было выяснено, что все типы эйкозаноидов инактивируются быстро, и их полувремя жизни составляет от нескольких секунд до нескольких минут. Простагландины инактивируются путем окисления гидроксильной группы в положении 15 до кетогруппы, способствующей их инактивации. Затем происходит β-окисление боковой цепи, а после него — ω-окисление. Конечными продуктами данного процесса выступают дикарбоновые кислоты, выделяющиеся с мочой.
Обобщая, можно сказать, что эйкозаноиды играют важную роль в биологических процессах, требующих быстрого ответа со стороны организма. Применение аналогов эйкозаноидов может быть эффективным в лечении различных заболеваний, таких как язвы желудка и двенадцатиперстной кишки. Однако, из-за быстрой инактивации эйкозаноидов, такие лекарства имеют короткий период действия.
